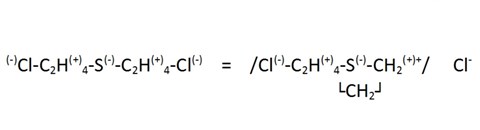Az előző részek:
Röviden a nukleinsavakról
Fontos: A cikksorozatom további részei előtt előrebocsátom, hogy ezekben a részekben számos olyan kitétel lesz, hogy arra jól képzett orvos, vegyész vagy egy molekuláris biológus összeráncolja a szemöldökét: „ez nem pontosan így van”, illetve „nos, ez ennél kicsikét bonyolultabb”. Tudom. De van terjedelmi korlát.
A közérthetőség és a követhetőség érdekében nem fogok belemenni olyan kémiai, molekuláris biokémiai részletekbe, magyarázatokba, amelyekbe szívesen belemennék, de tudom, hogy a többséget untatná, nem találkozik érdeklődésével, esetleg nem is értené meg. Végeredményben, olvasói kérésre, azért indítottam ezt a cikksorozatot, hogy elmagyarázzam, mi az, hogy oltás. Lehet, hogy messziről kezdtem, és látszólag még mindig messze vagyunk, de ugyebár a Karatekölyök c. filmben is a növendék hetekig csak autót políroz, és amikor pofozkodni kezd, akkor jön rá, hogy miért is. Egyszerűsítésre törekszem, és félek tőle, hogy sokak számára így is száraz és érdektelen lesz, de többen és többször mondták már nekem, hogy pl. vegyipari technikus képző évfolyamok számára is tudok úgy oktatni, hogy a gyerek a második órára már érdeklődve jöjjön be, úgyhogy optimista vagyok, mint b.szó baknyúl a vágóhídon. Persze, nem mindenki – egyszerűen az érdeklődési területek eltérnek. Engem meg rohadtul nem érdekel a szimfonikus zene például, vagy a „gendertudományok”.
A közérthetőség és a követhetőség érdekében nem fogok belemenni olyan kémiai, molekuláris biokémiai részletekbe, magyarázatokba, amelyekbe szívesen belemennék, de tudom, hogy a többséget untatná, nem találkozik érdeklődésével, esetleg nem is értené meg. Végeredményben, olvasói kérésre, azért indítottam ezt a cikksorozatot, hogy elmagyarázzam, mi az, hogy oltás. Lehet, hogy messziről kezdtem, és látszólag még mindig messze vagyunk, de ugyebár a Karatekölyök c. filmben is a növendék hetekig csak autót políroz, és amikor pofozkodni kezd, akkor jön rá, hogy miért is. Egyszerűsítésre törekszem, és félek tőle, hogy sokak számára így is száraz és érdektelen lesz, de többen és többször mondták már nekem, hogy pl. vegyipari technikus képző évfolyamok számára is tudok úgy oktatni, hogy a gyerek a második órára már érdeklődve jöjjön be, úgyhogy optimista vagyok, mint b.szó baknyúl a vágóhídon. Persze, nem mindenki – egyszerűen az érdeklődési területek eltérnek. Engem meg rohadtul nem érdekel a szimfonikus zene például, vagy a „gendertudományok”.
Kérem szépen, a nukleinsavakat, amelyek nevükben azért hasonlítanak a nukleáris fegyverekre, mert mindkét szó töve a latin nucleus, azaz mag, a sejtmag vegyszeres szétcincálása során Friedrich Miescher nevű nagyon ráérő svájci tudós fedezte fel 1869-ben, 25 éves korában, mikor más csak p.na után szaladgál. A vegyületekről megállapította, hogy savanyúak, mint a fent említett, ami után szaladgálni kellene neki, ezért sav, e mellett nagy mennyiségű nitrogént és foszfort tartalmaz. A felfedezést eltették a fiókba, mert nukleinsavból annyira kevés van az élő szervezetben, hogy annak biztosan csak valami lényegtelen, alárendelt szerepe lehet. Akkoriban mindenki bámulatosan hosszú fehérjemolekulákat keresett és csodált, hiszen már rájöttek, hogy a fehérjék sok-sok aminosavból álló, hatalmas molekulák, melyek tulajdonságai rendkívül változatosak, és viszonylag csekély hőmérséklet, pH, sótartalom stb. változásra elképesztő térszerkezeti változásokon mennek át, és így kb. kialakult az első sejtés arról, hogy miképpen is működik egy élő szervezet. Meg a döglött, mikor megemésztik…
Azt középiskolában is tanítják, hogy egy kiváló cseh szerzetes (megint az a rohadt elmaradott egyház…), Mendel leírta az öröklődési alaptörvényeket, csak mert nagyon szerette a borsót, de hosszú ideig senkinek nem volt arról fogalma, hogy a bizonyos tulajdonságok MIKÉPPEN is öröklődnek, mi ennek a tulajdonképpeni mechanizmusa. Lamarck még úgy gondolta, hogy a zsiráf, ha sokat nyújtogatja a nyakát, az megnyúlik,és a hosszú nyakú zsiráf sikeresebb, mint féllábú a s.ggberúgóversenyen, ezért nagyobb valószínűséggel adja tovább megváltozott tulajdonságait. Na igen, de tapasztalati tény, hogy a szerzett tulajdonságok nem öröklődnek, még a hülyeség se, pedig sokszor úgy tűnik. Egy Weissman nevű porosz biológus az 1880-as években nekiállt, és hatalmas kitartó türelemmel 1952 egér farkát vágta le 22 egérnemzedéken keresztül, hátha születik végre egy farok nélküli egér. Kitalálható: csak azt tudta bebizonyítani, hogy nem. Más kérdés, hogy a XXI. században már a nukleotidbázisok metilizációs mintázatának felismerésével ez a kérdés azért lényegesen „finomodott”. Erről később.
Szóval, 1900 körül, mikor lelkes fizikusok nyakra-főre rádiumsókat desztillálgattak, lelketlen sz.rkeverők pedig világháborút és a világ gazdasági és ideológia megszállását tervezgették, a lelkes biokémikusok szerették volna megtalálni, hogy mitől is öröklődik... a bármi. Bizonyára van valamiféle anyag, ami az örökítőanyag. Hol kell, hogy legyen az? Viszonylag nem nehéz rájönni, hogyha valaki töményen keresi az örökítőanyagot, másszon bele a spermiumba. Könnyű vele kísérletezni, mindig virgonc, és kéznél van, és kiköpött olyan, mint akiből származik, csak gyorsan kell kiköpni. Annyira leegyszerűsített szerkezet, hogy fruktózzal működik, szőlőcukorral nem is megy, mert még az az enzim is ki van belőle spórolva, ami a glükózból fruktózt csinál. Egy Martin Kossel nevű srác volt az, aki egyrészt felismerte a nukleotidok szerkezetét, és először gyanút fogott, másrészt pedig leírta, hogy a spermium nem más, mint egy rakat nukleinsav egy rakétafejrészben, és kb. az összes többi sejtalkotórész csak arra hivatott, hogy ezt a köteget mozgassa. Flemming, nem a penicillines, hanem egy másik, ez német volt, 1882-ben felfedezte a kromoszómákat, akkoriban volt újdonság a sejtfestés, és neki sikerült bacikban egy bizonyos kis testecskét megszínezni. (Kromosz - görögül - színes. Mint a króm vegyületei.) Innen már csak egy lépés volt, hogy kiszedjék a baktériumsejtből a kromatint, és azt tapasztalták, hogy a sejt SOHA nem osztódik, ha elszedik a kromatinját. Bingó. És mi van a kromatinban? Lepucolták róla a fehérjét, és a közepén ott figyelt a nukleinsav. Persze, még több mint ötven év kellett ahhoz, hogy Watson és Crick kimutassa a DNS helikális szerkezetét, és véglegesen bebizonyítsák, hogy ez az örökítőanyag. Akkoriban még ilyesmiért adtak Nobel-díjjat, nem lapostévé-rablásért. Azóta ezt buzeráljuk. Kivéve, mikor a víziló-izzadságot, mert nemrég egy kiváló biokémikus a víziló izzadságában (tessék elképzelni a kutatót, aki nap mint nap kis kendőcskével törölgette a víziló arcát, hogy mintához jusson) egy remek napvédő faktort fedezett fel (hipposuddorsav), és mihelyt semlegesíteni tudják a kivonat víziló-hónaljszagát, betegre fogja magát keresni ezzel a környezetbarát és nagyon hatékony naptejjel (ez most nem vicc, tényleg), de léteznek ennél fővonalbelibb kutatások is.
A ribonukleinsavnak és a dezoxiribonukleinsavnak, ezt ismételten középiskolában is tanítják, az alapszerkezetét egy ortofoszforsavval összekapcsolt, „összeészteresített” öt szénatomos cukor – ribonukleinsav esetén a ribóz, dezoxiribonukleinsav esetén a dezoxi-ribóz – hosszú-hosszú lánca adja. A cukrokat a 3. és 5. szénatomon köti össze a foszfáthíd. Az élővilágban nagyon elterjedt a különböző vegyületek különböző mértékben történő foszforizálása, egyszerűen azért, mert a szén-szén kötések hasítása nagyon energiaigényes, ezért sokkal takarékosabb, egyszerűbb és gyorsabb valamit foszfáttal kapcsolni össze, vagy ki, vagy be, azaz, az adott molekula tulajdonságait megváltoztatni. Az élő szervezetben amolyan 1.0., hogy egy enzimet úgy kapcsolnak ki-be, hogy foszforilizálják, ekkor a működése leáll, elteszik a polcra, ha megint kell, lehasad róla a foszfát, és újra működik. Az így létrejött lánc nagyon stabil. Építőelemként adja magát egy szénhidrát, a szervezet rengeteg-féle szénhidrátot használ (hát még a növények, fotoszintézishez! Olyanokat, amiről átlagember sose hallott, szeduloheptózt, eritrózt, stb.) ribózt azonban szinte semmihez, de fel tudja építeni, így nagyon adja magát, hogy nem az energetikai szempontból fontos cukrokból építkezik – az öt szénatomos méret különben is jobb.
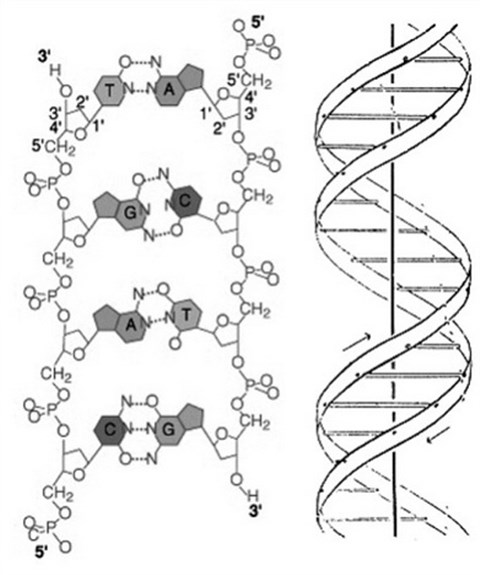
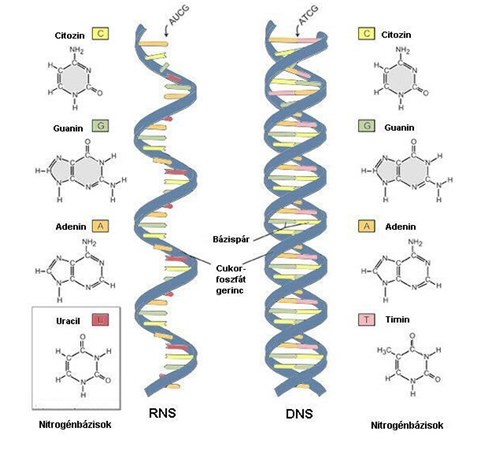
Erre az alapláncra kerülnek fel az ún. nukleotidbázisok (nukleotid az egy foszfátból, cukorból és nukleotidbázisból álló alapegységek, kvázi a DNS és az RNS téglái) akik a tulajdonképpeni kódot meghatározó molekulák. Ezek DNS-ben két purinvázú, az adenin és a guanin, és két pirimidinvázas, azaz hatos gyűrűs, ezek a citozin és a timin. Az adenin timinnel, a guanin citozinnal áll párba, ezt onnan lehet megjegyezni, hogy AT és GC párok vannak, azaz az örökítőanyag a spermiumban GC-t tartalmaz. Az RNS-ben másféle bázisok (ún. ritka bázisok) is vannak, és timin helyett uracilt tartalmaz, hogy miért, arról később. Szerkezetük az alábbi:
A nukleinsavak, ezt szintén tanítják középiskolában, felcsavarodnak egy spirállá. A DNS kettős spirált képez, azaz két komplementer (egymást kiegészítő) DNS-szál csavarodik egybe, mint említettem volt fentebb, úgy, hogy az egyik guaninjával szemben citozin, adeninjével szemben timin van stb. Az RNS az élőlényekben többnyire egy szálú. Vírusokban van kétszálú RNS – lám, a koronavírusban is. Az információt – a fehérjék szintéziséhez – a bázissorrend hordozza (meg más információt is).
(Na dióhéjjban ennyit a vulgármaterialista primitívségről, hogy a világban csak anyag van. Az egész élő létezés arra van felfűzve, hogy egy anyag kódol egy másikat, azaz információt – anyagon túli létezőt – rejt és használ. A világ – már csak ezért sem – nem csak anyag, szellem is, főleg szellem.)
Meg kell jegyezni, hogy az „ősi” nukleinsav minden bizonnyal az RNS volt. Az RNS tűnik régebbinek, mondhatjuk úgy, az originálnak. Először is, az RNS (pontosabban egyes RNS-ek) tud, tudnak enzimként működni (ribozinok), másrészt a DNS egyfajta továbbfejlesztésnek tűnik: nem használ ritka bázisokat, és kettős szálja stabilabb. RNS kettős láncot nagyon kevés kivétellel csak egyes ősi vírusokban találunk (pl. az influenzavírus is kettős RNS vírus). A spirális kettős lánc csavarodásához a dezoxi-ribóz molekula helyigénye miatt jobb, mint a ribóz. A kaliforniai Scripps Kutatóintézet munkatársainak 2008-ban sikerült olyan nukleinsav-analógokat (peptid-nukleinsavakat, úgynevezett PNS-eket, PNA-kat) előállítani, amelynek részegységei önmaguktól képesek összekapcsolódni. A folyamathoz nem volt szükség semmilyen enzimre. Megjegyzedő, hogy az RNS-ek tulajdonsága az un, elongáció, azaz, ha rövid, 3-10-20 bázist tartalmazó RNS molekulákat összekeverünk vizes oldatban, azok hajlamosak hosszabb láncokba rendeződni, kb. 100-200 bázisig. Ez meglehetősen furcsa, mert általában a molekulák maguktól inkább szétesnek, mint növekednek, mivel termodinamikailag ez a kívánatos, a logikus. A PNS-ak még ezt annyival fejelik meg, a kialakult szakaszok (oligomerek) képesek voltak dinamikus szekvenciamódosulásokra az oldatban lévő templátok (mintaként szolgáló molekulák) megváltoztatásának hatására. Ez a dinamikus szekvencia-adaptáció már az élő rendszerek jellemző tulajdonsága, azaz a „legősibb” forma ez a fehérje-RNS komplex lehetett. Majd fogunk arról szólni, hogy miképpen mutatják ki a szennyvízből a koronavírust: tessék majd akkor emlékezni az itt leírtakra.
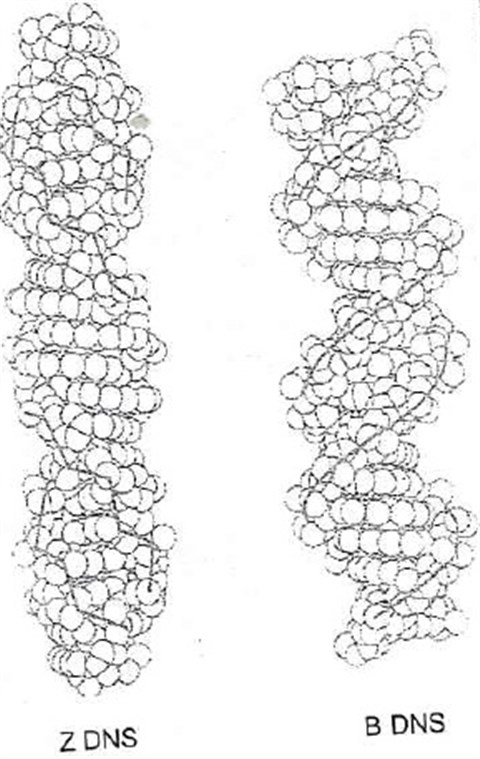
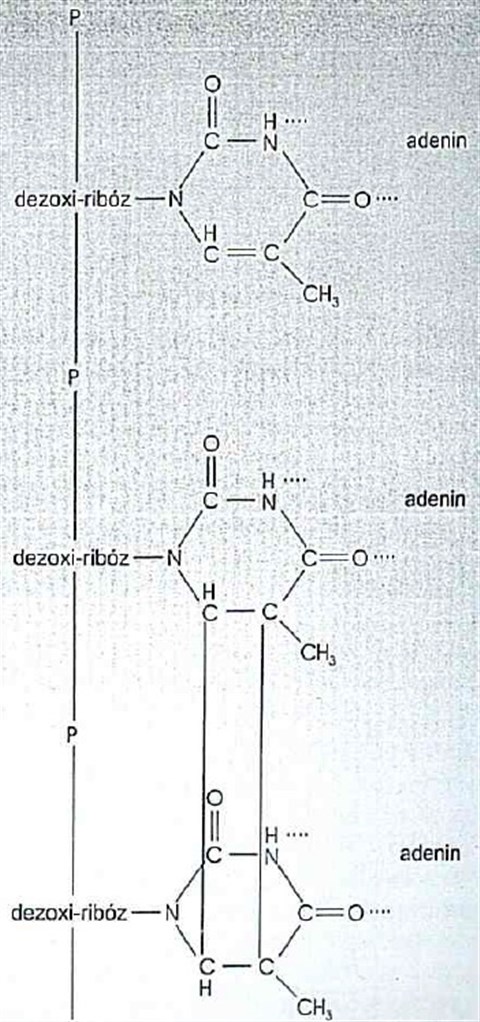
A DNS-ek marha hosszúak tudnak ám lenni, az ember teljes genomja letekerve 160 centi lenne, ez azért nemcsak harcsából, de molekulából elég komoly méret. Azt már nem tanítják, hogy míg a buzeránsok LMBTQ-k, addig a DNS-ek ABCZ-k szeretnek lenni, azaz, a molekulán belüli másodlagos kötőerők, energiaszintek több stabil konfigurációt (nem meglepő módon A, B, C, és Z szerkezetet) is lehetővé tesznek, és ezek egyikből a másikba alakulnak. Az átalakulásukat, ahogy csomagolásukat és leolvasásukat is, különböző fehérjék végzik, ezek „pattintják” egyik szerkezetből a másikba a DNS-t. A DNS leggyakrabban B formában van, ekkor 10 nukleotid ad egy teljes csavarulatot. A kettős spirál átmérője mintegy 2 nm, a bázisok távolsága a tengely mentén 0,34 nanométer, ez nem tűnik soknak, de molekuláris mértékkel mérve ez feltűnően sok. Ha környezetben alacsony a sókoncentráció,a DNS átmegy „A” alakba, ekkor nem 10, hanem 11 nukleotid ad egy csavart, „C” formában pedig 9. Ez kell ahhoz, hogy ilyen-olyan enzimek rá tudjanak illeszkedni. A „Z” („zig-zag”) forma elég speciális: ekkor a hélix balmenetes, ekkor a DNS hosszabb és vékonyabb. Egyes szabályzó szakaszokon ilyen a DNS, ezt a bázisok metilezése stabilizálja, erre azért van szükség, hogy a megfelelő szakaszok elkülönüljenek. Ezt kb. így kell elképzelni:
A sejtmagos élőlények (eukarióták, ideértve a növényeket, állatokat, gombákat, nyálkagombákat, állati véglényeket (ún. protisztákat)) DNS-e egy jó hosszú csík, pontosabban több, mert ahány kromoszómánk van, az annyi DNS, azaz az ember teljes örökítőanyaga 46 db DNS. (És ha már fogalmaknál járunk, a gén, az egy meghatározott szakasz egy kromoszómán, a genom pedig a teljes, komplett génszerkezet, minden gén együtt, azaz a teljes örökítőanyag-készlet). A csimpánzoké 48, mert a 2. kromoszóma a csimpánzoknál két darabban van, egyébként sok eltérés nincs, konkrétan a többin se. Éppen a kromoszómaszám nem egyezése miatt nem lehet embert csimpánzzal szaporítani, bár egyes embertársainkat elnézve ebben rendszeresen kételkednünk. Egyébként ennél genetikailag távolabb álló fajok is létre tudnak hozni (továbbszaporodásra nem képes) hibrideket, pl. az oroszlán és a tigris. (Biztosan ismerős a vicc, hogy a kici ócó kínai kutatócsoport majmot akar keresztezni emberrel, ehhez keresnek egy férfi jelentkezőt, százezer dollárban jelölve meg az akció díját, annak, aki erre hajlandó. Jelentkezik egy Kolompár Velociraptor, és mondja, ő vállalja, de három feltétellel. És mi lenne az? - Először is, teljes diszkréciót kérek – Ez természetes... – Másodszor: szeretnék én nevet adni az utódnak – Ez is megoldható – Harmadszor: részletekben szeretném kifizetni.)
A baktériumoké viszont gyűrűs. De ez a gyűrűs DNS másodlagosan is feltekercselődik. Ezért a baciknak van egy ezzel foglalkozó speciális enzime, a DNS topoizomeráz (giráz). De az ember ún. mitokondriális DNS-e is gyűrűs, többek között ezért is feltételezik, hogy a magasabb rendű szervezetek mitokondrium nevű sejtszervei valaha önálló baktériumok voltak, akik szimbiózisba léptek az állati és növényi sejtekkel.
A DNS-sel, amíg rendeltetésszerűen működik, két dolog történhet: vagy lemásolódik – megkettőződik – mert sejtosztódás történik – vagy lehívnak róla adatot, azaz RNS-t másolnak róla. Mást a DNS nem csinál, ül szépen a sejtmagban (sejtmagnélkül bacikák esetén csak úgy a plazmában), sőt, természetesen ezt se ő csinálja, ez történik vele.
A DNS megkettőződésének (átírásának, replikációjának, ahogy tetszik), hogy a spirál két szála elválik, és mind a kettőről (templátról) egy-egy kiegésztő (komplementer) lánc másolat készül. A két új DNS ezért egy-egy régi és egy-egy újonnan szintetizált láncból van, ezért nevezik őket semikonzervatívnak, mint a Neokohn portál olvasóit.
A natív DNS-t egyszerű melegítéssel is szét lehet választani. A két szemben álló bázist ugyanis másodlagos kötőerők, ún. hidrogénhíd-kötések tartják össze, ezek elég gyengécskék. Vizes oldatban melegítve, hogy a hidrogénhíd-kötések 50%-a felbomlik, azt mondjuk, a DNS „megolvad”, bár természetesen szó sincs arról, hogy folyékonnyá válna. Bámulatos, hogy lehűtéskor egy ilyen hatalmas molekula szépen vissza is tud rendeződni, de persze meg lehet trükközni. A Covid-járvány kapcsán elhíresült PCR-tesztekben is szerepe van ennek a dolognak, erről majd még később szólunk. A szervezetben azonban nem lehet rezsót tenni a DNS alá, ehhez még a b.zikban sincs elég meleg, ezért okos kis enzimrendszerek végzik ezt a munkát. A baktériumokban, ahol a DNS elég rövid, mert a genetikai információ se sok, és az is brutálisan tömörített, és a DNS kör alakú, azaz úgy néz ki, mint egy megcsavart biciklibelső, mikor Kari Geri ráül, egy helyen indul a másolás, az eukariótákban, ahol a DNS sokkal nagyobb, és a DNS-t a kromoszómákban ún. hisztonfehérjék tartják és veszik körül, sok ponton egyszerre indul el a másolás, különben kis túlzással a világvégéig nem végeznének, elképzelem, ahogy Mihály arkangyal éppen döfködi le a (kommunista) vörös sárkányt, meg a káromló tengeri vadállatot, az angyalok öntögetik kifelé a csészéiket, az önzés és a konzumidiótizmus nagy szajha Babilonja éppen dől összefelé, de bocs, várjunk még egy kicsit, mert nem végzett Józsi bácsi elivott májsejtjében a DNS polimeráz.
Bacikákban a mintául szolgáló „régi” DNS-láncról az új komplementer lánc szintézisét a DNS polimeráz III. enzim végzi. A polimeráz I. csak hibákat javítgat. A DNS polimeráz I. enzim egyetlen fehérjelánc, amely háromféle műveletet is végez, olyan, mint egy svájci bicska. Mindkét irányba menve tudja a DNS-t hasítani, és ki is tudja egészíteni. A géntechnológiában előszeretettel használják. Ráül szépen a láncra, és a DNS szerkezete alapján szépen megváltoztatja a harmadlagos szerkezetét, és a szerint dolgozik,hogy éppen ott és akkor mit kell. A polimeráz III., mint említettük, pedig új láncot csinál. Ehhez természetesen alapanyagokat – nukleotidokat – és megfelelő magnéziumion-koncentrációt kér, továbbá egy indító láncvéget, mert magától nem tud kezdeni. Ezt egy primáznak (nem primásnak, dikk) nevezett enzim biztosítja neki. (A sejtmagosok DNS replikációja némileg bonyolultabb...)
Értelemszerű, hogy a DNS lemásolásának marha pontosnak kell lennie. A villámszerűen gépelő titkárnő (sose csap jó helyre…) esete itt nem focizik. Baktériumokban a másolás közbeni láncjavítást maga a polimeráz III. végzi, A szintézis során beépített utolsó nukleotid minta DNS utolsó bázisa között, ha minden rendben van, létrejönnek a másodlagos hidrogénhíd-kötések, a két bázis szépen párba áll. Ezt az enzim egy meós része ellenőrzi, és ha minden oké, akkor a megváltozó elektronszerkezet miatt az enzimfehérje térszerkezete is megváltozik, és szépen elengedi a bázist, és eggyel továbblép. Ha ez nem jön össze, az utolsóként csatlakoztatott nukleotid hibás, bázisa nem komplementer a minta-bázissal, a polimeráz megáll, és visszalép, másik térszerkezetet vesz fel, és az utolsó kötést hidrolikusan (az észterkötéshez hozzáad egy vizet, két hidroxilcsoport keletkezik, és a molekula szétválik) elhasítja, és a hibás nukleotidot kidobja, és újratölt. Ezt egy másodperc alatt úgy pár százezerszer. Ezt követően azonban már nem tudja összekapcsolni a láncot, ezért megy „mögötte” egy másik enzim, a DNS ligáz, amely ezt elvégzi, a kötéshiányt (amit a molekuláris biológiai gyakorlatban „Nick”-nek hívunk, ezt onnan lehet megjegyezni, hogy mint Michael Douglas-t kb. mindegyik filmjében, pl. az Elemi ösztönben is, mikor Miss Stone bugyi nélkül keresztbe rakja előtte a lábikóit, ott a luk) befoltozza.
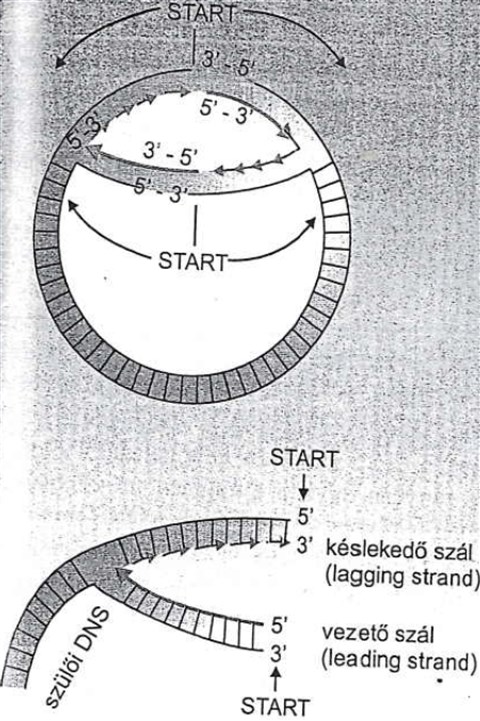
Ha már luk, akkor elképzelhetünk egy kör alakú baktérium-DNS-t. Hogy ez hogyan kettőződik, nos, leginkább úgy, ahogy a zipzárt lehúzzák (mondjuk Sharon Stone-ról, pláne 20-30 éve) és a két DNS szál között az egyik előrébb, a másik hátrébb jár, ezért beszélünk vezető (leader, de ha úgy jobban tetszik Führer) és késlekedő (lagging) szálról. Ezt lerajzolva lehet legjobban megérteni:
Sejtmagnélkül barátaink nagy gyűrűs DNS-e mellett rendelkeznek – többnyire egy picivel is, vagy adott esetben sok pici gyűrűvel, ezek csak pár ezer vagy pár tízezer nukleotidból állnak, míg azért, hát a baktériumok többsége meglehetősen ecccerű teremtés, de azért nekik is millió feletti bázispárjuk van, pl. az E. coli, mint általánosan használt fosató és biotechnológiai baci négymillió bázispárral mintegy 12 000 dolgot kódol, szóval, egyszerűbb, mint albán faék. Ezt a kis, kiegészítő DNS gyárát hívják plazmidnak, amit a biotechnológiában nagyon szeretünk. A plazmidok, a nagy DNS-től függetlenül replikálódhatnak, egy-egy baktériumsejtben több száz is lehet bennük. A plazmidoknak háromféle típusa van, az F vagy szexfaktor...bármennyire hihetetlen, a baktériumok is szexelnek néha…, az R vagy rezisztenciafaktort, és létezik egy ún. kolicinogén faktor, ez most a mi szempontunkból nem fontos.
Az a baci, aki termel egy F plazmidot, az egy kis nyúlványt is csinál hozzá, ezért őt tekintjük fiúnak, a nőnemű baci pedig az, aki ezt befogadja. A baktériumok még nem fedezték fel a nem-bináris LMBTQ/MZ/X nemi identitást. Az F faktor felnyílik, egyik szála átmegy a másik baciba, ott megszintetizálódik róla a komplementer lánc, és ezzel a baktériumok genetikai anyagot cseréltek, így az F- baktérium is F+ baktériummá alakul. Ezt követően a plazmid anyaga beépülhet a baktérium „nagy” DNS-ébe, ekkor beszélünk Hfr módosult baktériumról. A baci képes arra trükkre, hogy viszonozza a genetikai információ cseréjét, ő is adjon vissza valamit. Így pl. immunológia tulajdonságok nem csak kiszelektálódással, hanem ilyen trükkös módon is terjedni tudnak egy baktériumkultúrában (tiszteljük a baktériumkultúrát: sok embernek nincs egyéb kultúrája). A rezisztencia-plazmid szerepét taglalni se nagyon kell: ez többnyire bontóenzimek génjeit tartalmazza, amelyekkel a baktériumok vidáman tudnak védekezni antibiotikumok ellen. Ezek a rezisztenciafaktorok érdekes példát adnak: az „ugráló gének” jelenségét. Ezek mobil genetikai elemek, transzpozonoknak is nevezzük őket marha tudományosan. Ezek olyan DNS darabok, amelyek a DNS egyik helyéről másikra, vagy egyik DNS-ről a másikba kerülhetnek. Némelyik csak 2 gén, mások több tucat. Minden transzpozon obligát tartozéka saját enzimjének, a transzpozának a kódja, ez az enzim katalizálja a beékelődést (azaz amelyik kettőből áll, az egyik a transzpozáz). Tartalmaz továbbá a két szélén, bizonyos, fordítottan ismétlődő szekvenciákat, amelyek a gazda-DNS-be való beilleszkedéshez kellenek (inzerciós szekvencia, ezt onnan lehet megjegyezni, hogy intervenciós). Létezik olyan transzpozon, amely egy plazmiddal tud ugrani, és három nagyon kedves kis enzim genetikai kódját tartalmazza: a penicillint bontó béta-laktamázt, a klorocidot hatástalanító klóramfenikol-acil-transzferázt (nem káromkodtam) és a neomicint és a gentamicint elbontó foszfotranszferázt. Egyetlen R plazmid bemegy a baciba, és a baci egy csapásra egy gyógyszerkönyvnyi antibiotikumra lesz rezisztens, és az orvosnak leesik az álla, mint csodálkozó leprásnak. (Még szerencse, hogy a tetrán hatásos marad.)
Miért fontos dolog a plazmid? A biotechnológusok szempontjából azért, mert tulajdonképpen egy mesterséges plazmiddal baktériumsejtekbe vagy növényi sejtekbe nagyon sokféle idegen génszekvenciát nagyon hatékonyan és könnyen be tudnak, tudunk vinni. És ezt használják is, rutinszerűen. Az állati sejtekbe viszont nem épül be a plazmid, így plazmiddal ugyanolyan, sőt, jobb oltást lehet csinálni, mint mRNS-el (erről később). Ha az említett rezisztenciafaktorokat beteszik egy transzpozonnal összerakott plazmidba, akkor az adott baktérium kapásból rezisztens lesz az adott antibiotikumra, azaz a tenyészet egy nyakonöntéssel (az illetékes antibiotikummal) kapásból le is válogatható, hogy kik esetén sikerült a géntranszfer, kik esetén nem. Az átlagember számára a génsebészkedés rettenetesen elvont és bonyolult műveletnek tűnik. Holott tulajdonképpen meglehetősen egyszerű. Én pedig holnap viszem a kocsimat elektromos szerelőhöz, mert nekem meg marha bonyolult kivenni és kicserélni egy klímajeladót. Én meg arra nem vállalkozom. Biztosan azért, mert a bacik magukat összerakják, az autó meg nem. Szétszedni meg semmit se bonyolult…
Az eukarióták, a többsejtűek DNS-ének replikációját illetően több enzim és szaályzófehérje (hiszton) dolgozik. Itt csak egy dolgot emelnék ki: a hosszú, lineáris DNS-t tartalmazó eukarióta sejt kromoszómájának végeit telomereknek nevezzük. A telomerekben a DNS 3’-as végén a szál túlnyúló (telomer) vége guanin nukleotidot rengeteget tartalmazó, többször ismétlődő szekvenciákat tartalmaz. Amikor a DNS-t éppen nem másolják, ez a DNS vég egy kábelvégfogó fehérjével meg van fogva. Ugyanis, mikor a lineáris DNS-t másolják, a késlekedő lánc (tessék visszalapozni) 5’-végén jelentkezik egy kis gond: Mivel, mint említettük, a polimeráznak kell egy indító szakasz, a láncvégi indító RNS kimetszése után nem pótlódik a helye DNS-el, így a késlekedő lánc egy picurit rövidebb lesz, mint a mintául szolgáló, másolt DNS. Hogy az információt hordozó DNS szakasz ne vesszen el, a végére egyszerűen hülyeség van írva, ez a telomer, amely minden egyes sejtosztódáskor megrövidül. Ezt a szervezet úgy védi ki, hogy a egy speciális enzim, a telomeráz ezt a szakaszt visszaépíti. A telomeráz egy nagyon érdekes enzim, mert nem csak fehérjelánc, hanem van egy beépített RNS szakasza, ez a mintalánc, erről szintetizálódik egy komplementer telomer szekvencia, és az enzim ezt rakja be.
A felnőtt testi sejtekben a telomeráz már nem aktív, ezért DNS-ük minden egyes osztódáskor megrövidül. Ezért a magasabb rendű szervezetek, szemben a baktériumokkal, sejtjeiket tekintve, nem tudnak korlátlanul osztódni. Addig osztódhatnak, míg a DNS-ük végén tart a telomer. Ha a telomer szakasz elfogy, a DNS értelmes része rövidül, ezért a sejt max 1-2 osztódást bír még, degradálódik, majd elpusztul. Például, ha alkesz Jóska folyamatosan szétissza a máját, nem hal meg azonnal, de a májsejtek, hogy pótolják a pusztuló májsejteket, egy darabig osztódnak, aztán már nem tudnak. Onnantól már csak a kötőszövet tud osztódni, és a máj elfogy. Ezért mondjuk, hogy éveink száma és biológia életkorunk nem feltétlenül azonos, és hogy harmincon túl mindenki, igenis, felelős azért, hogy néz ki, hogy a szervezetét mennyire harcolta le! (Lehet neki átültetni egy másik májat, hogy azt is eligya.)
De jó lenne, ha aktívan tudnánk tartani a telomerázt, nem öregednénk meg! - gondolja az ember. És ez így is van. Nem öregednénk meg, mert a kontrollálatlanul szaporodó sejtjeink okán szépen meghalunk rákban, fiatalon. A rosszindulatú daganatok sejtjeiben a telomeráz rendszerint ismét aktív: ezért szaporodhat korlátlanul a ráksejt. Ebből három dolog következik: egy, elméletben volna lehetőség univerzális rákgyógyszert felfedezni, csak azt nem egyszerű. Kettő, a biotechnológiai munka, gyártás szempontjából, ha emberi (állati) szövettenyészetet kell alkalmazni, a gyakorlatban rendszerint egy rákot használnak. Pl. az egyik leggyakoribb emberi szövettenyészet egy hetvenes évekbeli laphámrák. Ez szaporítható, egy darab, találomra kivett emberkedarab meg nem. És három, ezért (is…) 1.0. hülyeség, hogy „a GMO rákot okoz”, mert DNS-ra ható (karcinogén) anyag nélkül egy mesterségesen bevitt DNS darab sosem fog tudni rákot okozni, mivel szükséges, hogy a telomerázt kikapcsoló gént „kiüssék”. Ez mutatja, hogy mennyire sok sérülés kell a DNS-en, hogy annak rák legyen a vége, találomra ezt is el kell találni. Besugárzás, karcinogén hatására sokkal valószínűbb, hogy a sejt elpusztul a DNS károsodása miatt, minthogy korlátlan szaporodásba kezdjen. És a javító mechanizmusok teljesítménye óriási, egy átlagemberben naponta több milliárd DNS károsodás történik, amit ezek kijavítanak, és az immunrendszer és a beépített „programozott sejthalál” mechanizmusok a sérült sejteket az esetek igen nagy százalékában kiszűrik, becslések szerint egy átlagember naponta több száz ráksejtet képez, de ezeket a rendszer általában eliminálja (ezért rákkeltő a stressz, mert az immunrendszer működését visszavető stressz ezt akadályozza). A p53 jelű gén egy speciális fehérjét kódol. EZ a fehérje addig „fogja” a sejtmagot a sejtosztódás S fázisában, míg a reparáló mechanizmusok be nem fejeződtek. A p53 fehérjéje a sejtekben nagymértékben felszaporodik, ha a sejtet besugározzák, vagy rákkeltő anyagoknak teszik ki. Ha pedig a sérülések nem javíthatóak, akkor elindítja a programozott sejthalált. Ha a p53-as gén kiesik, a mutánsok látszólag egészségesek, de fiatalon meghalnak daganatos megbetegedésekben. Így lehet pl. rövid élettartamú kísérleti egereket előállítani. Lehet GMO-val rákot okozni, ha beviszünk egy olyan gént, hogy az adott sejt kezdjen el rákkeltő anyagot termelni – de csak így, és nem másképpen.
Mint említettem, a DNS másolás meglehetősen pontos. Ha nem volna az, kevéssé hasonlítanánk szüleinkre, és kb. úgy néznénk ki, mint a csernobili állatkert. Annak, aki kitalálta a nukleinsav-alapú öröklődési rendszert, olyan szerkezetet kellett csinálnia, ami meglepően stabil, de ettől függetlenül meghatározott, nagyon csekély (mikrorizikós) valószínűséggel képes változni, mert az is kell, különben még mindig archeaként legelésznénk a piritkristályokon, és az sokkal kevésbé finom, mint a brassói aprópecsenye. Tehát léteznie kell mutációs lehetőségnek, de ennek nagyon aprónak kell lennie. Márcsak azért, mert a mutáció ritkán hasznos, ahogy pl. egy jól kitalált belsőégésű motor se valószínű, hogy jobb lesz attól, hogy Móriczka véletlenszerűen átír valamilyen tervezési adatot.
Sérülés hatására roncsolódhatnak a DNS bázisai, vagy elveszhetnek, de ez a ritkább, gyakoribb, hogy a foszfordiészterkötések elhasadnak, a szálakon belül vagy a szálak között keresztkötések alakulnak ki. Ha a károsodás egy adott szakaszon a DNS lánc csak egyik szálát érinti, az a replikáció előtt többnyire kijavításra kerül, mert az éppen maradt komplementer őrzi az eredeti információt. Ha a javítás a replikációig nem következik be, a változás rögzül, ekkor beszélünk mutációról. Nagyon leegyszerűsítve a dolgokat, egy többsejtűnél, egy állatnál, ha a testi sejtet éri mutáció, defektusos lesz vagy rákos, ha a csírasejtet, akkor az utód károsodik. Genetikai értelemben hatékonyabb dolog a nőstényeket besugározni. A csernobili és a hirosimai tapasztalatok azt támasztották alá, hogy mivel a hím a szerelem oltárán kis farkincások százmillióit áldozza fel, a nyomorékok ezek közül nem éppen gyorsak (régi duma: „nem tudom elhinni, hogy százmillió sperma közül te voltál a legéletképesebb!”), valószínű, hogy egy „jó” fog célba érni, addig a cél-petesejt károsodása végzetes. Ezért gyakori idősebb (40 éven felüli) anyák gyerekei esetén a Down-kór és más születési rendellenességek, mert a petéik már több mutagénnek voltak kitéve. Ezért is lenne fontos, hogy a nők 17-23 éves korban szüljenek, és utána akarjanak továbbtanulni, meg „karriert” csinálni, mert az ráérnek 45 évesen is, babázni meg nem. De ezt a nyugati társadalmak nem fogják fel, az eredmény meg látszik: fogyatkozó népességszám.
A DNS sérülését okozhatja sokféle dolog. Leginkább a gyakorlatban különböző vegyszerek, mérgek, vagy a nagyenergiájú, nagyfrekvenciájú (tehát rövid hullámhosszú) elektromágneses sugárzás, a néhány elektronvoltnyi energiájú UV fotonoktól fölfelé, a röntgen-, és gammasugárzás (megjegyzés: az ezekhez képest elképesztően hosszú hullámhosszú, csekély energiájú mikrohullámú-, és rádiófrekvenciás sugárzás NEM, az 5G nem okoz DNS károsodást, mert bolhaf.sznyi energiája nincs hozzá. Ami nem jelenti azt, hogy a megfelelő teljesítményű mikrohullámú sugárzással ne lehetne egészségkárosító hatást elérni, de az nem ÍGY fejti ki a hatását. A minimális energia, hogy a legérzékenyebb DNS bázisból (a guaninból) sikerüljön kilökni egy elektront, ahhoz a 285 nm-es hullámhosszú sugárzás szükséges. Az az ultraviola fény fertőtlenítő sávjának kezdete, az ún. Dornó-sugárzás. Az ennél rövidebb hullámhosszok energiája értelemszerűen még nagyobb, tehát ugyanúgy alkalmas, de a 280 körüli hullámhossz kitüntetett, mert ezt a DNS jól fel is veszi. Ezért a fertőtlenítő UV lámpák, az ún. germicidlámpák 230-260 nm-es hullámhosszon sugároznak. Ezen alapul a napfény fertőtlenítő hatása is, ezért nem terjed a gonosz koronavírus a júliusi napon a strandon fetrengve, és ezért hagyja nagyobbrészt békén a szaharai országokat, és pl. Brazíliában szépen kirajzolódik, hogy hol mekkora a napi átlagos felhőborítottság, mert azt mutatja a koronavírus-térkép, ugyanis a vírus terjedésének gátlásához nem meleg kell, hanem erős, közvetlen napfény. Ugyanezért nem terjed 2000 m felett se, ahol az erős UV szépen lepörköli, mert az erős, közvetlen napfényt a kórokozók nem bírják, minél apróbbak, annál inkább nem bírják, a vírusok főleg nem bírják (amit a biológiai fegyverekben úgy oldunk meg, hogy a vírustartalmú aeroszolhoz UV/fényvédő és stabilizáló faktorokat kevernek, az átlagember sose gondolná, hogy a naptej hadászati jelentőségű alapanyag) Sose felejtem el, mikor még boldogult bakancsos tiszti hallgató koromban szobatársam és kiváló cimborám gennyes pattanásainak kezelésére a doktor őrnagy úr a Honvédkorházban germicidlámpát írt fel, és egy békés januári vasárnap este a kollégiumi körletben (Porthos kommentelőtárs közben a szemközti folyosón ultizott) szépen süttette magát az UV lámpával, meg engem is, aki a szomszéd ágyon feküdtem és az otthoni folyékony barack segítségével viszonylag korán elaludtunk, és az UV lámpa, amivel 20-30 percet kellett volna napoznia, egész éjjel bekapcsolva maradt. Másnap reggel hólyagosra égve jelentünk meg a sorakozón, ami januárban nem mondható évszaknak megfelelő kinézetnek. Sajátos humor szolgálatvezetőnk közölte, hogy a lámpát adjuk kölcsön a nigériai apától származó Musztafa hallgatónak, mert nagyon hóka szegény.
Összehasonlításképpen: az 280 nm körüli UV sugárzás fotonjainak energiája pár tized elektronvolt, a „kemény” gamma-fotonoké kilo-megaelektronvolt tartományú, azaz ennek akár a tízmilliószorosa is lehet (a 260 GHz-es mikrohullámé pedig az UV foton energiájának ezredrészét éri el). Az UV sugárzás, mivel relatíve csekélyke energiájú, nem hatol mélyre a szövetekben. Bacikákat, vírusokat kinyír, és tud bőrrákot okozni, de mély szövetkárosító hatása nincs. Megjegyzendő, hogy az ionizáló (gamma, röntgen) sugárzás – amely viszont meg jó mélyre megy, mert energiája, az van hozzá - általában nem közvetlenül roncsolja a DNS-t, („találatelmélet”) hanem a vizet bontja, és a felszabaduló aktív oxidatív gyökök fogják a károsítást előidézni („vízaktivitás”). Ezt viszonylag nem nehéz bebizonyítani: liofilezett (azaz mélyfagyasztott, majd mélyfagyasztás után vákuumban bepárolt, más szavakkal instant) baktériumok sugártűrése általában kb. százszorosa a vegetatív baktériumoknak (egyébként a biotechnológiában rutinszerű a műanyag szerelékek, egyszer használatos eszközök gamma-sterilezése). Különben a telelő, hibernált, nem aktív állatok is nagyon bírják a radioaktív sugárzást: egy atomháború után tavasszal előmásznak a sündisznók, végignéznek a füstölgő romokon „hová tűnt itt mindenki, b.ssza meg?” arckifejezéssel a tüskés buksijukon. Ja, és egy tévhitet eloszlatandó: a csótányok nem bírják kiválóan a gamma-sugárzást. Igazság szerint a rovarok közül pont, hogy a csótányok a legérzékenyebbek.
Rengeteg vegyszer rákkeltő, közöttük teljesen természetes növényi hatóanyagok is. Ezért is hülyeség, hogy „de a gyógytea biztosan nem árt, szemben a gonosz gyógyszergyárak rohadt gyógyszereivel”. Például a nádálytő és a tüdőfű pirrolizin-vázas alkaloidái is, többek között, pedig ezek mostanság sztár-gyógynövények. Persze, azért az emberek DNS károsodásait azért nem ezek okozzák, sokkal inkább a króm, a benzol, na meg a koromra tapadó kondenzált benzolgyűrűs vegyületek. Remek rákkeltők a mustárgázok is. Ahogy az emberek pár millió évvel régebb óta b.sznak, minthogy ismernék a fogamzás hormonális mechanizmusát, úgy a kénmustárt úgy szórták nyakra-főre az első világháborúban egymásra a szemben álló felek, hogy fogalmuk se volt arról, hogy hogyan hat. Igazság szerint már az 1860-as években előállították, és hamar rájöttek, hogy ezzel az anyaggal nem lehet viccelni, és gyorsan kukázták is, egészen 1914-ig, mikor változott a szemlélet, és pont ilyen anyagokat kezdtek keresni. Adta magát a kérdés, hogy a viharba’ lehet egy ilyen egyszerű molekula háromszor-ötször mérgezőbb, mint a cián?
Egyszerűen. A kén-, nitrogén-, bróm-, és egyéb mustárok ikerionos szerkezetet vesznek fel, egyébként ezt is tanítják középiskolában, csak nem mustárgázzal.
A kénmustár kémiai, biokémiai és fiziológiai tulajdonságait, viselkedését speciális molekulaszerkezete magyarázza. A molekulán belüli C-Cl kötés igen erősen poláris, bár ez a legtöbb szerves vegyületnél nincs így. A kötést ugyanis a kénatom elektronvonzó képessége polarizálja, így a kénen és a klóron elektronfelesleg (parciális negatív töltés) a szénen elektronhiány (parciális pozitív töltés) van. Ennek megfelelően az elektrofil reakciók a molekula két végét és közepét, a nukleofil reakciók a kénmustár-molekula szénláncait támadják. Az elektroneloszlás alapján érthető, hogy a kénmustár könnyen végrehajt intramolekuláris átrendeződést, és ciklikus szerkezetű szulfonium-ion képződik belőle:
Ez az ionos szerkezetű forma magyarázza a kénmustár igen jó felszívódását a bőrről, és toxicitását is. Ez képes alkilezni a DNS bázisait, ezzel megakadályozni annak normál működését. És mivel a természetes repair mechanizmusokat nem mustárgáz ellen tervezték...
1919-ben észlelték első ízben a háborús veteránok, a mustármérgezettek egy részénél súlyos csontvelőkárosodás, leukopenia kialakulását. Megfigyelték a csontvelő és a nyirokszövet teljes pusztulását, feloldódását, amely akkor menthetetlenül halálos kimenetelű volt (ma már csontvelő-átültetéssel megmenthetőek lennének). Ez alapján nevezték el a hólyaghúzó harcanyagokat és származékaikat radiomimetikus anyagoknak, mivel vérképzőszereket károsító és mutagén hatásuk nagyon hasonló jellegű a radioaktív anyagok, az ionizáló sugárzás hatásához. A kémiailag nagyon aktív alkilező ágens, a kénmustár, a nitrogénmustár és származékaik károsítják a DNS-t és az RNS-t, ezért a legintenzívebben szaporodó sejtek – a csontvelő, a gonádok, és persze, a rákos sejtek – érzik meg a hatást legjobban. Egyébként a nitrogénmustár rákgyógyszerként is bevezetésre került, egyes származékai (pl. mannomustin) ma is használatban vannak mint kemoterápiás szerek. Először 1942-ben használták a mustárgázt egy limfomás betegnél: meg ugyan nem gyógyult, de átmenetileg drámai javulást hozott – ez indította meg a rákgyógyszerek kutatását. A kénmustárt kenőcs formájában (psoriazin) egyes rosszindulatú rákos bőrbetegségeknél és egyéb kórképeknél (pszorázis) ma is használják. Persze, ma már sokkal jobb rákellenes készítmények vannak, ezek az alkilező ágensek kb. azt a szintet képviselik, mikor húszkilós kalapáccsal akarunk motorvezérlőt javítani.
A DNS bázisai teljesen maguktól is tudnak mutálódni. Hasonlóan, ahogy a tizenöt éves Rézműves Pandémiát sem kell erőszakkal kirugdosni a kocsisorra, megy az magától is. Rézműves Pandémia unokahúga tehet erről, akit úgy hívnak, hogy Enol-oxo Tautoméria. Egyébként jelzem, ezt is tanítják középiskolában. Elviekben.
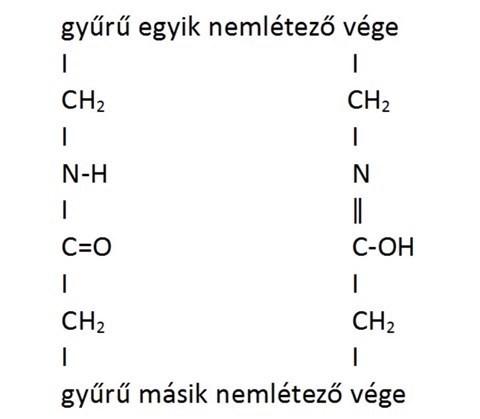
Bizonyos molekulák többféle szerkezetet is magukénak tudhatnak, és egyikből a másikba oda-vissza tudnak alakulni. Amíg csak a térbeli szerkezetüket csavargatják, ebben nincs meglepő, de bizonyos molekulák a kötéseiket is hobbiszinten változtatgatják. Tipikusan ilyenek azok a gyűrűs szerves vegyületek, ahol a gyűrűben nitrogén van, és a nitrogén mellett olyan szénatom van, amihez oxigén kapcsolódik. Ebben az esetben ők, mármint a nitrogén és az oxigén gyakran nem tudják eldönteni, hogy kihez is tartozzon a hidrogén, ahogy Gazsi és Zsiga is összevesznek, hogy kinek is a romnyija Rostás Preferencia. Azt hiszem, ezt is egyszerűbb lerajzolni:
Aki már középiskolában is inkább focizott, minthogy szerves kémiát lapozgasson, annak elárulom, hogy a szén mindig négy vegyértékű, aki ettől eltérőben gondolkozik, az vagy megbukik, vagy Nobel-díjjat kap, mint pl. Oláh György, de utóbbi most más kérdés. Alapesetben (itt és középiskolában nem ismertetendő kivételekkel) pedig a hidrogén egy, az oxigén kettő, a nitrogén pedig három (vagy öt) vegyértékű, és ebből kell hozni a kirakóst. És mivel ez nagyon sok variációt enged meg.
Szóval, nagyon kicsi a valószínűsége, hogy a bázis éppen a ritkábbik tautomer alakjában legyen, de megvan, és ekkor a szintáz rossz bázist tesz a helyére. Minden külső beavatkozás nélkül.
Nitrogéntartalmú heterociklusos vegyület pedig rengeteg van, kapásból, ha valaki iszik egy kávét, az azzal betermelt koffein ugyanúgy ilyen, mint a húgysav, amit majd maradékként kipisál a delikvens. A DNS-t és az RNS-t építő bázisok is ilyenek. Mikor bekötnek a molekulába, és kialakították a hidrogénhíd-másodlagos kötéseiket, onnantól a hidrogén röghöz kötött, mán’ nem megy sehová, mint a példában szereplő Rostás Preferencia se, mikor éppen Kalocsán üdül, a női fegyintézetben, félrebarátkozni csak akkor tud, mikor szabad. Gondolom, eléggé világos, hogyha a bázis akkor kerül enzim által megfogásra és beépítésre, mikor éppen a másik izomerének helyzetében van, akkor nem fogja tudni a stabil izomerének hidrogénhíd-kötését kialakítani, és a szembepárja nem lesz jó. Ha a repair mechanizmusok nem veszik észre, magától is megváltozik.
A leggyakoribb DNS károsodások a depurinizáció, a bázisok oldalláncainak dezaminálódása, dimerek képződése vagy nukleotidok kiesése, vagy lánctörés, keresztkötés.
Igen gyakori, hogy pl. UV fény hatására a szomszédos timinbázisok összekapcoslódnak. Néha citozinok, vagy timin-citozin párok között is előfordul. A depurinizáció azt jelenti, hogy a purinbázis (adenin vagy guanin) kiesnek, és csak a bázis nélküli dezoxi-ribóz marad a láncban. Faragó Anna azt írta: ez annyira azért nem gyakori, az emberben ez naponta tízezerszer fordul elő – sejtenként! Azaz, ennyiszer sérül a DNS csak ilyen módon, tehát egy átlagos szaporodó sejtünk repair mechanizmus nélkül napota tízezerszer, más szavakkal kb. kilenc másodpercenként beadná a kulcsot. Jó, mi?
A dezaminálódás vegyszerek, kegyszerek vagy radioaktív sugázás hatására következik be, a bázis „elhagy” egy aminocsoportot. Tudjuk, hogy az RNS a „régebbi”, az „ős” nukleinsav, ezért is mások a bázisai. A citizin, ha dezaminálódik, ott uracil keletkezik, az uracil viszont szembepárjának nem guanint, hanem adenint vonz, azaz egy ilyen dezaminálódás megváltoztatja a kettős spirál szekvenciáját. De a DNS-ben uracil helyett timin van, ezért az uracil ott értelmetlen, a javító mechanizmus kidobja, és jónapot. Ezért – és a dexoxi-ribóz jobb térszerkezeti tulajdonságai miatt – stabil a kettős DNS lánc, és sokkal kevésbé stabil a kettős RNS lánc.
A javítás mechnaizmusának leglassúbb folyamata a sérült bázis felismerése. Az ezzel foglalkozó endonukleáz megy szépen végig a szálon, és ahol illeszkedési hibát talál a hidrogénkötések alapján, kiemeli a sérült bázist. Mögötte halad egy, a bázis nélküli dezoxi-ribózt felismertő AP endonukleáz, amely kimetszi a maradványt, majd mögötte meg egy DNS polmeráz, amely befoltozza a lyukat, végül pedig a DNS ligáz, amel összeköti őket, azaz eltünteti a „nick”-et. A DNS polimeráz másolási tévedéseinek utólagos javítását a szakirodalomban „mismatch repair”-nak nevezik.
Ennek a javításnak jónak kell lenni, de soha nem tökéletesnek, mert akkor nem tudnának létrejönni változások, nem születnének mutációk, és az élőlények nem tudnának alkalmazkodni. Tehát az örökítőanyag „be van adjusztálva” egy olyan megbízhatósági pontra, amely lehetővé teszi az élőlények stabil fennmaradását (a külső behatás nélküli hibázási valószínűség kevesebb, mint 1010 átírás, repairral, persze) de ha a külső környezeti strasszfaktorok, körülmények – amelyek nyilván majd változásokat igényelnek az élet fennmaradása érdekében – a mutációs rátát adott esetben brutálisan megemelik (pl. 200 cGy besugárzás tízezerszeresére) – akkor megvan az a rugalmasság, amely ezt elengedi. Ebbe belegondolni is kemény, nem is sikerül mindnekinek.
Meg kell említeni, hogy azt, hogy egy anyag – akár egy gyógyszer, akár egy bármilyen technológiában használt vegyi anyag, egy növényvédőszer, vagy bármi, a kiskutya kabátja mennyire rákkeltő, mennyire mutagén, mennyire magzatkárosító (ún. CMR anyag) annyira azért nem bonyolult tesztelni. Ennek a módja az ún. Ames-próba. Erre a célra egy rokkant, hikomat Salmonellabacit használnak fel. Ez a jószág egy mutáció miatt elvesztette a képességét arra, hogy a hisztidin nevű aminosavat szintetizálni tudja, azaz, olyan szintetikus táptalajon, amelyben nincs hisztidin, nem életképes, de ha adnak neki, akkor köszöni, remekül van. (A hisztidinnek semmi köze a hisztihez, ez nem egy női baktérium.) Fogjuk a vizsgálandó anyagot, hozzákeverjük a tenyészethez. Ez a hisztidin-szintézis képtelenség egy eléggé banális hiba, és ha az adott anyag hat a DNS-re, akkor igen-igen nagy a valószínűsége, hogy rendbehozza a hibát, és a sok milliárdnyi tenyészeten lévő baci közzül egy véletlenül megjavul, mint a moszkvicsmotor a kalapácsütéstől. Ez után, ha a társaságot a hisztidinmentes táptalajra oltják át, akkor valaki életben marad, és elszaporodik, jelezve, hogy ez az anyag, amivel nyakon öntöttetek, nekem jót tett, de nektek nem biztos, hogy ilyen szerencsétek lesz, mert aki itt mutációt okoz, az okoz máshol is, és ráb.szhattok. Továbbá: az emberi szervezet meg olyan trükkös, hogy a májacskánk a bejutott rettenetes mérgeket mindenféleképpen szét akarja szedni, azaz az X. vizsgált anyagból valamiféle lebontott terméket csinál – és mivel csak az nem hibázik, aki nem csinál semmit – lehetséges, hogy amit előállít, az veszélyesebb lesz, mint ami eredetileg volt.
Hogy egy alap-példát hozzak, maga a benzpirén nem rákkeltő, de a máj megpróbálja oxidálni, mert mégiscsak egy büdös kátrány a szentem, ne legyen már a szervezetben, csak sajnos, amit csinál belőle, az 1,2-benzpirén-epoxid, az már piszkosul rákkeltő. Ezért ezt az Ames-próbát úgy is megismétlik, hogy előbb a vzsgálandó új fejlesztésű anyagot megrágatják eg komplett P450 citrokróm enzimrendszerrel, amely a májban is nekiugrana, és a a termékeket is megvizsgálják a Salmonellán. Ha nevezett bacin az anyag nem bizonyult DNS károsítónak, igen nagy a valószínűsége, hogy nem az. Ezt a próbát jó közelítéssel 15 éve már minden újonnan szintetizált anyagnál elvégzik. Így a gonosz mérgező harcanyag-szakértők egyre újabb és újabb DNS károsító anyagokhoz jutnak, mert aki kibukik, abból vegyi fegyver lesz. Mindenkit le kell lombozzak: a TCDD dioxinnál jobbat… nem találtak.
Tehát a korszerű gyógyszer-, és növényvédőszer-kutatás viszonylag gyorsan és egyszerűen ki tudja zárni DNS károsító, mutagén, ezzel potenciálisan rákkeltő anyagokat az előtt, mielőtt azokat állatkísérletnek vetnék alá, vagy emberrel kontaktusba kerülnének. Nem kell fosni minden új gyógyszertől, elég a ricinustól.
És még valami: nem tudom egyébként nem megjegyezni, és én mindig is nagyon csodáltam az ateistákat, akik tényleg elhiszik és meggyőződéssel vallják, hogy egy fél tucatnyi replikációenzim, tucatnyi kiszolgáló és transzporfehérje, szabályzófehérje hihetetlenül pontos és nagyszabású munkáját, olyan módon, hogy egy negyedleges szerkezetes enzim apró pH és sókoncentráció-eltérésekkel „megszabályozva”, de visszaható, önbeállító, önszabályzó rendszerekkel, pakk, csak úgy létrejön a nagy semmiből. Nem véletlen, hogy kozmológusok és molekuláris biológusok között nem szokás kételkedni abban, hogy ugyan, kérem, ez nem lehetséges. Vagy nevezett istentagadó jószágoknak egyszerűen csak fogalmuk sincs minderről, és nincs intelligenciájuk rendszerben gondolkodni, és ilyen összefüggéseket átlátni és megérteni? Valószínű. Sir Isaac Newton ezt négyszáz éve úgy fogalmazta meg, hogy aki egy icipicit iszik a tudás poharából, az megrészegül tőle, aki viszont kiissza, az a pohár mélyén úgyis meglátja az Úr arcát, és onnantól már megint csak úgy tud védekezni, ha behunyja a szemét.
A következő részben arról tervezek írni, hogy miként csinál a sejt saját magát saját magából saját magának a genetikai kód alapján, hogy mi is az az mRNS, és mi ebben a szerepe, mert korunkban az átlagpolgárnak a Messenger csak a fosbukról ismerős.
Vérnyúl
(A szerző olvasónk.)
Felhasznált irodalom:
J. Watson: A gén molekuláris biológiája
P. Karlson: Biokémia
Ádám Veronika: Orvosi biokémia
Bonta János: Műszaki egészségügyi sugárvédelem
Guba Ferenc: Orvosi mikrobiológia
P. Karlson: Biokémia
Ádám Veronika: Orvosi biokémia
Bonta János: Műszaki egészségügyi sugárvédelem
Guba Ferenc: Orvosi mikrobiológia