A korábbi részek:
V. rész: És hogyan is lesz a fehérje – mit csinál az a gonosz mRNS?
Az élő szervezetek, mint tisztáztuk, szerkezetüket tekintve gyakorlatilag fehérjékből állnak. Mint ahogy a középiskolában tanítják, az élő-, és félőlények fehérjéi alapvetően húszféle aminosavból épülnek fel, amelyekhez persze, egyéb molekulák is kapcsolódhatnak, metilizálódhatnak, módosulhatnak, illetve a bonyolultabb fehérjék több fehérjeláncból állnak - általában diszulfidhidakkal kapcsolódnak össze – ilyenek többek között, nagyon sok más fehérje mellett az hemoglobinok és azok az immunglobulinok is, amelyek a szervezet fertőzésekkel szembeni védekezésének fontos eszközei, és ezért pl. kovid-fertőzések során is a rá, mármint a gonosz koronavírusra jellemző immunglobulinokat (Ig) igyekeznek kimutatni több-kevesebb sikerrel.
A húsz aminosavon kívül ismertek egyéb aminosavak is, de azok nagyon ritkák, és nem „láncba szintetizálódnak”, hanem a már készült lánc alakítódik át.
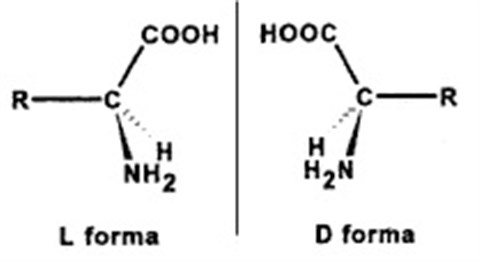
A természetes aminosavak nagyon kevés kivétellel L-konfigurációjúak, azaz balra forgatóak. Ha aminosavakat mesterségesen állítunk elő – ideértve nemcsak a megszokott gyártási módszereket, hanem a híres-elhíresült Urey-Miller féle kísérletet is, mikor az őslégkör és az ősóceán körülményeit megidézve egy szervetlen leveskét kevergetve elektromos kisülésekkel kezelt és többek között aminosavakat kapott – az opitikailag nem aktív, racém, L,D vegyes aminosavat kapjuk eredményül. Ha a természetben is így lenne, negyven (2 x 20) aminosavat kellene kódolni az RNS-eknek, mert mindenki duplán számítana, viszont nem működnénk.
(MÉR? Bár középiskolában ezt is tanítják (tanítani kéne…) de azt hiszem, pár szóval erre is ki kell térni. Ha veszünk egy olyan bármilyen tárgyat, amelyben ún. kiralitáscentrum van, azaz a gyakorlatban egy olyan pont, amihez legalább négy eltérő térszerkezet kapcsolódik, akkor legalább kétféle módon fel lehet építeni úgy azt a tárgyat az azonos alkotókból, hogy az ne legyen azonos. Molekulák esetén ezt hívjuk optikai izomeriának. Hogy ezt egy kézenfekvő példával illusztráljam, tessen szíves lenni ránézni a két kicsi dolgos kezére. Egyforma a két keze? Nem.
Bár ugyanúgy néznek ki, fedésbe akkor se hozhatóak, ha a Szent István-i vagy a hagyományos iszlám büntetőpolitika alapelveinek megfelelően lenyesnénk őket lopás után. A két kézfej egymás tükörképi párjai, hogy csúnyán káromkodjak, eantimerjei, de nem egyformák. Nem lehető őket úgy forgatni, hogy fedésbe kerüljenek egymással. Egy három vegyértékű központi atommal rendelkező molekulát, pl. egy metil-etil-amint nem lehet úgy megcsinálni, hogy az összes molekula ne legyen bármelyik másikkal fedésbe hozni, a három csoport ehhez ugyanis kevés. De a négy már igen. Ezért egy négy kötéssel rendelkező szénatom, ha hozzá négy különböző csoport kapcsolódik, kétféle optikai szerkezetet vehet fel, mint a két mancsunk is. Még olyan rettentő egyszerű molekulák is, mint a fluor-klór-bróm-metán (halon 1111) is két eantiomert képez, és a glicin kivételével mindegyik aminosavnak lehet jobbra és balra forgató változata (amely molekulák oldatban a polarizált fény síkját tényleg el is forgatják egyébként, azaz nem brahiból hívják őket így).
Megfigyelhető a biokémiában, hogy rendszerint mindig csak az egyik változat „ér”, a másik többnyire nem focizik, pl. az atropinnak is két térszerkezeti izomer keveréke amelyikből az egyik halálos méreg, mert beköt a receptorhoz, a másik meg nem köt be, és ezért nem is hat. De még csak nem is hét. (Ha az emberek olyan alapvetően nem túl bonyolult dolgokkal tisztában lennének, minthogy ahhoz, hogy valami bekövetkezzen, ahhoz szükségszerűen valamiféle változás szükséges, egy élettani hatáshoz tartozik egy hatásmechanizmus, minden, élettanilag aktív molekulának elő kell idéznie valamiféle változást, ehhez neki minimum jelen kell lennie... akkor pl. a homeopszichopaták szépen éhenhalnának a sarlatán ráolvasásos-lötyögtetett birinéne-kotyvalékaikkal, és csak a valódi gyógyszergyártók lennének a piacon - az ő kotyvalékaikkal.
A legegyszerűbb glicin kivételével minden aminosav optikailag aktív, és mindegyikük L. Ennek összetett okai vannak, ennek ismertetése itt végkép nem cél terjedelmi okokból. Ez alól kivételt jelent a gonosz-gonosz antraxbaktérium, amely tokja pofátlan módon jobbra forgató (D) aminosavakból, pontosabban glutaminsavból áll. Ezért minden fehérjebontó enzim visszapattan róla, közlik, hogy erre nem terjed ki a munkaköri leírásuk, ezért elképesztően ellenálló az antraxbaktérium, és évtizedeket tud pihenni a talajban vagy Oszama bin Laden fiókjában. Véletlenek – nincsennek.)
Mint megbeszéltük, a nukleinsavak alapvetően négy bázist használnak, azaz olyan ábécéjük van, ami négy betűből áll, tehát talán még egy kongói átlagpolgár is elboldogulna vele. Lehetséges-e húsz aminosavat leírni négy betűvel? Ez Fegyőr Bandikáék szellemi képességeit meghaladó kérdés, de talán a legbutább cigánygyerekét nem: nem lehet. És két betűvel? Négyszer négy, az 16 variáns – hát, ez is még kevés. És hárommal? Az már 43, azaz 64, annyi elég, átlagban mindenkire jut három kód is! Ennyi elég, hozzátéve, hogy nem 20, hanem 21 jelet kell kódolni, mert szükséges egy „állj le, b.szdmeg” jelzés is, amit stopkodonnak nevezünk. Startjel nem kell? Lehetne startjel is, de az a nagy büdös helyzet, hogy tervezőnk a maga kifogyhatatlan humorával úgy intézte a dolgokat, hogy minden fehérje metioninnal (bacik esetén N-formil-metioninnal) kezdődik, így arra nincs szükség. Azaz három bázispár kódol egy aminosavat, ezért nevezzük őket bázistriplettnek, és mivel átlagban mindenkire három jut, így egy aminosavnak több triplett is megfelel. Igazság szerint csak a már említett metioninnak (AUG) és a triptofánnak (UGG) van egy kódja, stopkodon is három van (UAG, UGA, UAA) a három kódos izoleucin kivételével mindenki másnak 2 vagy 4 kódja van. Ezek mindig hasonlóak, sőt, a hasonló aminosavaké is hasonlóak, így, ha esetleg leolvasási hiba vagy mutáció lépne fel, az esetek többségében az nem jelent tényleges fehérjeszerkezet-megváltozást, azaz a genetikai információ megváltozása tulajdonképpen rejtett marad, nem manifesztálódik (pl. a CC a harmadik bázistól függetlenül minden esetben prolint jelent). A kód egyetemes. Néhány nagyon elb.szott „evolúciós zsákutca” mélytengeri herkenytű és primitív ősbaktérium, valamint a mitokondriumjaink kivételével az egész élővilág ugyanazt használja. Ez önmagában döbbenetes, de én szívesen elkapnék egy ufókot, hogy a kis szürke nagy szeműek is ugyanezt használják-e. Nem tudom, mi lenne a megdöbbentőbb: hogy nem, létezhet másféle kódolás is, vagy ha ugyanez van nekik is...
Ott hagytuk abba, hogy az mRNS elkészült a maga szerkezetében, amelynek az elején van egy rövid nem kódoló szakasz, majd ez után az első AUG bázishármassal elindul a fehérjelánc kódja. Az mRNS folyamatos, az AUG („iniciátor kodon”) után nincs szignál meg kávészünet, ha egy 100 aminosavas láncot kell legyártani, akkor az AUG után további 297 bázis jön, majd egy stopjel, utána pedig már szintén tárgyalt „farokrész”. Az eukariótákban az mRNS természetes formája azonban nem egy hosszú lánc, hanem egy gyűrű, mert a vége visszakapcsolódik a „cap” fehérjébe, ami az elején található, így ez a gyűrű védett minden bontóenzimtől, amíg meg nem érkezik a fehérjeszintetizáló apparátusba, azaz a riboszómába. Ezért, míg a baktériumokban gyorsan elbomlanak az mRNS-ek, az eukarióta sejtekben az mRNS-ek életideje, amíg nem kötöttek be egy riboszómába, meglehetősen hosszú, adott esetben napokban, hetekben mérhető, míg egy baktériumban percekben. Ha egy mRNS esetleg sérült, elromlott, hibás, ami megeshet (mivel, mint említettük, az RNS-re átírásnak, szemben a DNS kettőződéssel NINCS hibajavító mechanizmusa) akkor nem tud becsatlakozni a riboszómába, és viszonylag hosszú ideig ottmarad. (Ezt nem nagyon szokták túlhangsúlyozni, mikor az mRNS oltások esetleges hatásairól szó esik.) A mesterséges, az oltásokban alkalmazott mRNS-ek azonban bázisaikat tekintve, így elbontásukban is – eltérnek a természetes mRNS-ektől. Ezért élettartalmukat is más tényezők szabják meg.
A baktériumok és az eukarióták riboszómái sokban eltérnek, de mindkettőre igaz. Hogy egy kisebb és egy nagyobb fehérje-alegységből állnak össze, melyek molekulatömege közel 3 millió (az eukariótáké több molekulából áll), és saját, benne működő r (riboszóma) RNS-ek vannak benne, amelyek szerkezete eltér az mRNS-től. Amíg a riboszóma „nem dolgozik”, addig nincs összekapcsolódva, az akkor következik be, mikor beköt hozzá az mRNS, és a molekulaszerkezet megváltozik, és a riboszóma munkába áll. A riboszómák sejten belüli „terelgetését” kisméretű, ún. scRNS-ek végzik.
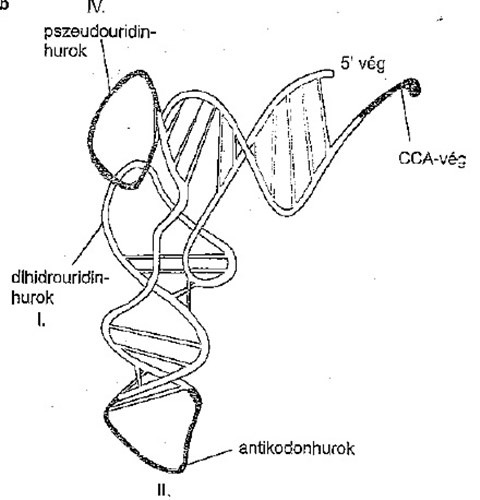
A riboszómák szerkezete az mRNS, az aminosavakat beadagoló t(transzfer)RNS és a riboszóma-fehérjék térszerkezet-változásai folyamatosan, lépésről lépésre összerakja a peptidláncot. A transzfer RNS sokban eltér a többi nukleinsavtól. Először is, nagyon speciális térszerkezete van, másrészt a többi nukleinsavhoz képest viszonylag kicsi molekula. Ezen kívül nemcsak a négy „klasszikus” bázist tartalmazzák, hanem speciális, ritka bázisokat is. A tRNS leginkább látszólag egy összegubancolt vezetékre emlékeztet, amit Gazsi is inkább szétvágna, mint kitekerne. Ezt a térszerkezetet éppen speciális bázisai másodlagos kötéseinek köszönheti, a 3-as végén pedig, mint a megfázás elleni szernek ACC (adenin, citozin, citozin) a bázissorrendje (de mivel a sorendet a másik végétől számoljuk, ezért ezt CCA végnek hívjuk). Ettől a CCA végtől legtávolabbi hurok a molekulán az ún. antikodon hurok, amely hét nukleotidból áll, és ez az, amelynek a három belső nukleotidja a tulajdonképpeni kulcs-zár, amely felismeri az mRNS három nukleotidos szakaszait, amelyek az aminosavakat kódolják. Minden aminosavnak más-más tRNS felel meg, de nem minden kódnak van saját tRNS-e. A tRNS-ek zárja olyan kitágult, mint egy harminc éve pályán lévő prostituált, ezt a jelenséget ezért egyébként „kodon-antikodon lötyögésnek” nevezzük, azaz pl. a valint kódoló GUU és GUC, GUA, GUG hármasok közzül kb. mindegy, melyik jelenik meg, az jó lesz. Ezt is némi molekulaszerkezet-módosulással éri el a tRNS. A tRNS egy enzimnek (aminoacil-tRNS-szintetáz) segítségével a kódjának megfelelő aminosavat ragadja meg, és szépen beilleszti a láncba. Természetes körülmények között csak egyféle aminosavat foghat meg, de szintetikusan lehet rá más aminosavat is illeszteni. Nem gatyázik, akkor azt rakja be. (Mint az előző részben említett enyhén beállt lengyel vendégmunkások a BMW gyárban.) Az mRNS a riboszóma kis alegységéhez kötődik, a startjelhez (a metionin AUG kodonjához) hozzáilleszkedik az iniciátor tRNS antikodonja, ezt nevezzük szép szóval 30S iniciciós komplexnek. A kialakulásához egy rakás segítő fehérje, az un iniciációs faktorok szükségesek. Ezek akadályozzák meg hogy azt „üres” riboszóma, amibe nincs belehúzva…a….nem az, hanem az mRNS, ne tapadjon össze. Ezért ezeknek a fehérjéknek a „kilövése” speciális mérgekkel szintén nagyon jó sejtgyilkoló módszer. Él ezzel pár antibiotikum.
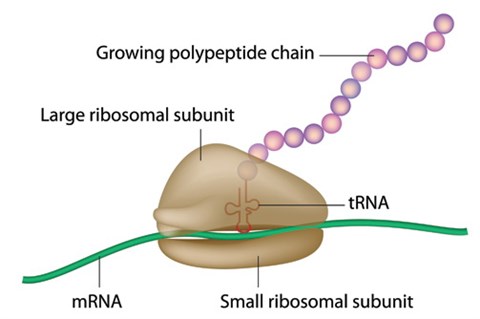 Sematikus ábra a fehérjeszintézisről: a riboszóma két alegysége közzé beilleszkedő mRNS-ről a tRNS-ek másolnak, nagyszámú segítő fehérje közreműködésével (forrás: pmlive.com) |
A polipeptid láncának szintézise, a lánc hosszabbodása, rohadt okosul mondva elongációja ciklikusan ismétlődő három lépésből áll. Első lépésben a polipeptid második aminosavát (ugye, az első a metionin, ő már be van töltve) hordozó aminosav-transzfer-RNS kötődik be az aminoacil kötőhelyre, a második kodonnak megfelelő pozícióban illeszkedve. Az aminoacil-tRNS bekötődése energiát igényel, magától nem megy végbe, ezért (sem) tudunk kaja nélkül nőni, ezt is, mint szinte minden energiát igénylő folyamatot az élő szervezetben, nagyenergiájú trifoszfátok hidrolizálása biztosítja, de itt nem az általában használ adenozin-trifoszfát (ATP) bomlik, hanem egy guanin-trifoszfát, és a bekötést egy másik fehérje („elongációs faktor”) hajtja végre, ez köti meg és hasítja a GTP-t. Egy másik faktorfehérje a GDP-vé bomlott GTP maradékot lehajítja az elongációs testvértő’. Ez pár nanoszekundumot vesz igénybe, pont annyit, hogy a szintézisfejen ellenőrizhető legyen, hogy a kodon és az antikodon passzolnak, azaz, tényleg ez az aminosav kell-e, amit az adott tRNS hozott. Kicsit olyan, mint mikor Lakatosné megmossa a kis Gazsi arcát, mielőtt enni ad neki, hogy biztos, hogy a saját purgyéja-e? Ha ez megvolt, és Gazsi, izé, a kodon passzol, akkor jó, ha viszont nem, az egész rendszer szétesik, és újra próbálkoznak. A második lépésben a már betöltött metionin és a következő, második aminosav között létrejön a peptidkötés. Ez külön energiát nem igényel, mert mikor az aminoacil-tRNS bekötődött, annak a kötési energiája felhalmozódott, és az aktiválja a két aminosavat, ide GTP nem kell, de kell egy enzim, a peptidil-transzferáz (ezt is meg lehet bénítani, és akkor is megdöglik a sejt. Kiváló erre az arzén, de az egyébként sok más enzimet is likvidál, nem véletlenül vált be méregként. De szelektíven teszi ezt a klóramfenikol, ezért ez is remek antibiotikum, csak az embergyógyászatban már betiltották, mert nagyjából azért többé-kevésbé az emberben is megcsinálja, így nem ép ártalmatlan, de viszont nagyon széles hatású. Léteznek olyan antibiotikumok, amelyek rettenetes erős mérgek, ennél is durvábbak. Ezeket csak olyan fertőzésben adják, amikor kb. már minden mindegy. Van olyan, amely klinikai tapasztalatok szerint 16% valószínűséggel májrákot okoz. Az nem piskóta, de egy olyan fertőzésben, a mely viszont 100%-ban halálos, és más meg nem hat, mindenki elfogadja, és reméli, hogy nem rá fordul az orosz rulett, mert az esély pont ugyanakkora. ) Amikor kialakult a peptidkötés, a legelső, a metinint hozott tRNS leválik, és a második tRNS fogja le a láncot….már amennyire lánc még két aminosav. A harmadik lépés pedig az, hogy a riboszóma egy peppet odébb gördül az egészhez viszonyítva. Az AUG kodon és a már kiürült, metionint hozott tRNS leesnek. ekkor a riboszóma „rágördül” a harmadik aminosavat kódoló tripletre, és az egész folytatódik tovább.
Mint említettük, a bacikban vannak nagyon hosszú mRNS-ek, (policisztonok) akik több aminosavat is kódolnak, a fejlettebb élőlényekben egy mRNS = egy fehérje. Ezért értelemszerűen a policisztonos mRNS-en a lánc között is van stopkodon (biztos, ami biztos, általában egymás után több is…) az eukarióta mRNS-eknek azonban csak a legvége előtt.
Érdekes, de egy riboszóma kb. 80 nukleotodnyi hosszúságú. Ha egy riboszómát az egyszerűség kedvéért úgy képzelünk el, mint egy nem szabályosan kettévágott almát, amelybe egyik irányból be van húzva egy cérna (az mRNS) a másik irányból egy összegubancolódott cérna (A tRNS) akkor az alma 80 egységhosszt takar el az egészből. Ha az mRNS ennél hosszabb, ami valószínű, hiszen 80 nukleotid ugye, max 26 aminosavat kódol, ami elég cseppecske fehérje, akkor a vége túllóg a riboszómán. Ezért egy mRNS-en egyszerre több riboszóma is dolgozhat, sőt, rendszerint dolgozik is, az mRNS nem egy géppuskaheveder, hogy végigszalad, lefut, és annyi, hanem egész riboszóma-nyáj vonul rajta végig, és közben mindenki gyártja, húzza róla le a fehérjét.
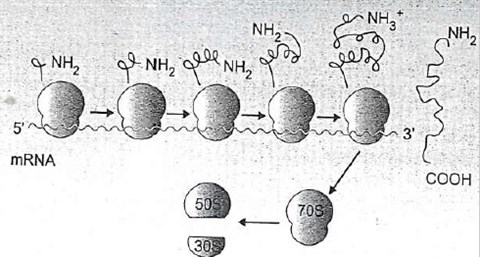 Az egymást követő riboszómák ugyanarról az mRNS-ről gyártanak fehérjét, egymástól függetlenül, ez a képződmény az ún. poliszóma (forrás: Ádám Veronika és munkatársai: Orvosi mikrobiológia) |
Megjegyzendő, hogy pl. a sztreptomicin a baktériumokban az egyik riboszóma fehérje meghülyítése révén elrontja a leolvasási kódot, és így a sztreptomicinnel kezelt baktérium nem tud fehérjét szintetizálni, és megmurgyel. Viszont ezt egy viszonylag egyszerű mutációval ki tudja védeni, sőt, létezik olyan riboszóma-fehérje, amely rövidlát, akkor pontos, ha van mellette sztreptomicin. Az ilyen baktérium nemhogy megdöglene az antibiotikumtól, hanem keményen függő a szerencsétlen, csak sztreptomicin jelenlétében tud szaporodni. A tetrán, a tetraciklinek pedig az aminoacil-tRNS bekötődését gátolják meg. Mivel ezek a folyamatok kissé másképpen folynak le baciban, mint emberben, a tetránok úgy ezerszerte mérgezőbbek baktériumra (már amelyikre…) ezért alkalmasak gyógyításra.
Magyarán szólva, ahhoz, hogy bármely sajtunk, elnézést, sejtünk bármilyen fehérjét legyártson, ahhoz mRNS léte nem kerülhető meg, tehát ez egy alapvető fontosságú csatorna, igazság szerint már nagyon régen érett az a biotechnológiai igény, hogy erre a mechanizmusra ráépítsenek. Éppen ideje volt.
A vírusok is ebbe a ventillátorba igyekeznek belehugyozni, és az itt és az előző részben elmondott metódusba érdeklődnek bele, hogy ezt a saját céljaikra fordítsák, arról tervezek írni legközelebb. És ezzel megérkeztünk a témához, mondhatja az olvasó, hogy egy hónap után ideje volt. Szerintem ezeket el kellett mondanom, mert unos-untalan vissza fogok hivatkozni rájuk.
Végezetül adnék egy gondolkodtató feladatot. Tessék elképzelni egy 100 aminosavból álló, tehát meglehetősen egyszerű, egyláncú fehérjét. Ennél bonyolultabb tízezer féle van a legtrógerebb baktériumban is. Hány variációban létezhet 100 aminosavból álló fehérje, ha húszféle aminosav építi fel? Logikus: 20100-on, azaz ez megfelel 2100 x 10100-nak. Szép nagy szám.
Mennyire nagy? Nos, az elképzelhető legnagyobb átviteli sebességű enzim olyan nagyjából, nagyságrendileg 1014 másodpercenkénti átviteli számmal dolgozik, de ez elképesztően kivételes. Tételezzük fel, azt a hülyeséget, hogy az egész világegyetem komplett, úgy ahogy van, nemcsak a csillagokat, de beleértve a sötét anyagot és a sötét energiát is, aminosavkeverékből áll, ideálisan elegyítve, tömege tehát 1055 g, és a világegyetem kb. 14 milliárd éves, ami megfelel 4,34 x 1017 másodpercnek. Más szavakkal, a világegyetem életkorának milliárdszorosa és milliárdszor milliárd világegyetem még bőven-bőven kevés statisztikailag ahhoz, hogy egy ilyen fehérje „úgy véletlenül” létrejöjjön, még ha lenne hozzá egy elméleti, minden variációt legyártani igyekvő hipotetikus peptidáz is, aki persze, nem lehet ott, mert mivel ő ennél egy sokkal-sokkal bonyolultabb fehérje, az ő létrejötte ennél még pár százezermilliárdszor pár százezermilliárdszor pár százezermilliárdmilliárdszorosan valószínűtlenebb. Nem életről beszéltünk, hanem csak egy nyúlpöcsnyi fehérjéről, amely úgy viszonyul a legegyszerűbb bakteriális élethez, mint egy pici csavar egy cirkálóhoz. Gondolkodó ember itt kényszerűen belátja: statisztikailag nem létezünk. Vagy legalábbis: az ismert alapvető materiális fizikai, kémiai, biológiai folyamatok és törvényszerűségek az élet létrejöttét önmagukban – nem magyarázzák meg. Se ebben a példában, sem máshol. Világról alkotott ismereteink egy ponton megállni kényszerülnek: ott, ahol egy ezen túli, másféle szabályrendszer áll.
Egyébként pont ugyanez igaz a részecskefizikára és a kozmológiára is, biztosan tök véletlenül, tehát nem kell aggódni azért, hogy nincs a világegyetemben élet, mert egyébként világegyetem sincs. Mármint, ha a materialistáknak igazuk van, és nincs út, igazság és élet.
Vérnyúl
(A szerző olvasónk.)
Irodalom:
P. Karlson: Biokémia, 1972
Ádám Veronika és Munkatársai: Orvosi biokémia, 2010
J. Watson: A gén molekuláris biológiája, 1980
Pál Tibor: Orvosi mikrobiológia, 2020
Bruckner Győző: Szerves Kémia, I-2, 1982
Ádám Veronika és Munkatársai: Orvosi biokémia, 2010
J. Watson: A gén molekuláris biológiája, 1980
Pál Tibor: Orvosi mikrobiológia, 2020
Bruckner Győző: Szerves Kémia, I-2, 1982